日前,曹鹏研究员团队在国际疼痛学会会刊、疼痛领域顶级期刊PAIN上在线发表了题为 “A sting of scorpion Buthus martensii Karsch targets Nav1.7 in mice and mimics a phenotype of human chronic pain” 的研究论文。揭示了药用动物东亚钳蝎蝎毒致痛的关键分子机制。该论文的通讯作者为曹鹏研究员,卢悟广副研究员为第一作者,参与本研究的有来自耶鲁大学医学院的程晓阳研究员、Stephen G. Waxman教授、中国药科大学的于烨研究员等,南京中医药大学为第一单位。

蝎、蜈蚣等产毒动物为血肉之品,有情之物,性喜攻逐走窜,通经达络,搜剔疏利,无处不至;又与人类体质接近,容易吸收和利用,效用佳良而可靠,起到挽澜之功,乃草木、矿石之类所不能比拟,被中医临床广泛使用。产毒动物分泌毒液引起其天敌或猎物产生剧烈的疼痛甚至瘫痪是其重要的生存策略,举着毒螯在地球上行走了4亿年的蝎子正是其中的佼佼者。尽管已有多种蝎毒多肽被鉴定具有致痛活性,但是其致痛的机理仍不清楚。
电压门控钠通道(VGSC)对疼痛感知至关重要,伤害感受器是周围神经系统的感觉神经元,主要表达Nav1.1、Nav1.3、Nav1.6、Nav1.7、Nav1.8和Nav1.9通道亚型。人类和小鼠的遗传学研究表明,Nav1.7在疼痛信号传递中扮演关键角色,使该通道成为开发镇痛药的有吸引力的目标。然而,由于使用敲除小鼠的研究存在局限性,以及缺乏有效的Nav1.7选择性激活剂和抑制剂,Nav1.7在疼痛信号传导中的确切作用仍然值得深入研究。
该研究首次证实Nav1.7是药用动物东亚钳蝎蝎毒致痛生存策略的关键靶标,蝎毒通过增强Nav1.7的活性产生疼痛效应,并分离鉴定了蝎毒中与Nav1.7相互作用的关键成分, 长链毒素Makatoxin-3。
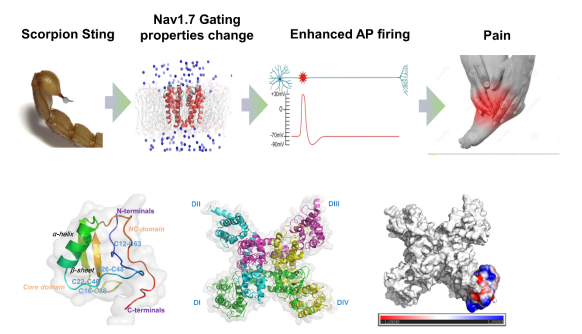
Makatoxin-3通过作用于 Nav1.7电压敏感结构域4(VSD4)表面的S3-S4环,抑制Nav1.7快速失活,从而增强动作电位发放,导致疼痛阈值降低,引起疼痛。以上发现表明东亚钳蝎毒液可作为新型的离子通道探针库用于Nav1.7调节剂的筛选。Makatoxin-3与Nav1.7的相互作用模式将为设计新型Nav1.7特异性的激动剂或Nav1.7靶向镇痛药提供新的思路。
工作得到国家自然科学基金优秀青年基金(81622048),国家行业专项-名贵珍稀动物药全蝎、蟾酥及混伪品鉴定技术及规范应用研究(201507002-11)等项目资助。

