我院江苏省中药高效给药系统工程技术研究中心近年来致力于智能型仿生多功能纳米药物递送系统的构建,着力解决中药复方生物利用度低、病灶部位靶向性差等问题,为中药活性组分的高效递送以及复杂疾病的精准治疗提供思路。团队王若宁副教授研究小组在狄留庆教授指导下在国际知名学术期刊ACS Nano(IF:18.027,中科院分区1区)在线发表最新研究成果。
由于血脑屏障(blood brain barrier, BBB)和血脑肿瘤屏障(blood brain tumor barrier, BBTB)的存在,大部分候选药物无法有效地蓄积在脑胶质瘤病灶部位。此外,免疫抑制微环境也是脑胶质瘤治疗的一大阻碍。因此,多策略联合克服胶质瘤的治疗阻碍至关重要。基于前期工作基础(Acta Pharmaceutica Sinica B. 2022, Journal of Controlled Release. 2022. 2023, Journal of Medicinal Chemistry. 2022, Journal of Nanobiotechnology. 2020),发现血清来源的外泌体(Exosome,EXO)表达有丰富的TfR,其可以通过与血液中游离的转铁蛋白结合,进而靶向大脑。由于EXO是内源性物质,所以相比于其它常用的纳米载体具有更低的免疫原性,并且能够逃避单核巨噬系统的吞噬,从而实现在体内的长循环。传统中药丹参中的脂溶性活性成分与甘草中的两亲性活性成分可通过自组装策略构建纳米胶束(TanⅡA-GL nano-micelles, TGM),同时发挥不同组分间的协同治疗作用。受EXO独特理化性质启发,团队将在EXO表面修饰了免疫佐剂CpG ODN 1826,成功构建了脑胶质瘤靶向及化疗、免疫治疗一体化的仿生纳米递送系统,用于递送纳米胶束(TGM),以“Immune Exosomes Loading Self-assembled Nano-micelles Traverse the Blood-brain Barrier for Chemo-immunotherapy Against Glioblastoma”为题发表于ACS Nano上。该研究制备所得荷载中药自组装胶束的“免疫外泌体”纳米粒,可以有效改善单一载体药物荷载量低、生物相容性差、靶向穿透力弱、治疗机制单一等问题,能够精准靶向脑胶质瘤病灶部位,通过化学疗法和免疫疗法协同治疗脑胶质瘤,在未来具有广阔的应用前景(Fig. 1)。
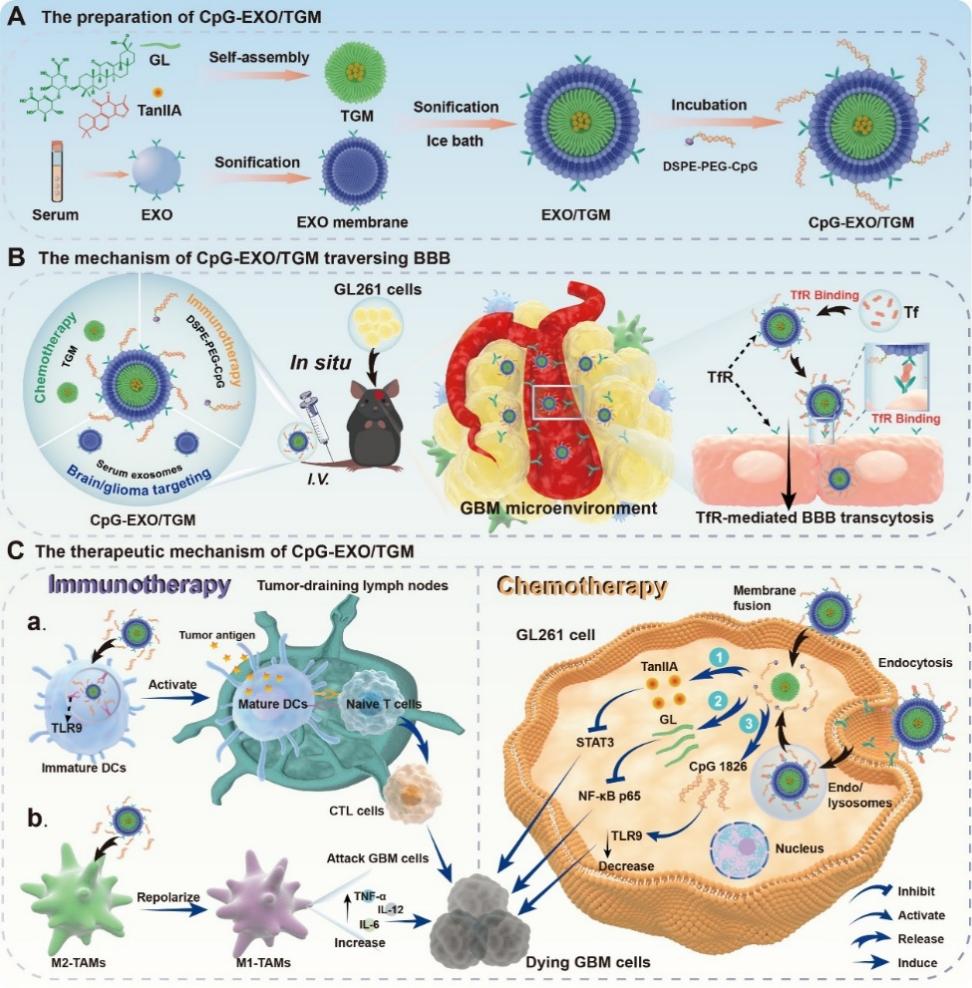
Fig. 1. The "immune exosome" nanoparticles of traditional Chinese medicine self-assembled micelles, CpG-EXO/TGM, treated brain glioma together through chemotherapy and immunotherapy.
上述研究获得国家自然科学基金(81903557、82274104、82074024)、江苏省自然科学基金(BK20190802)、江苏省高等学校自然科学基金(19KJB350003)、江苏省科协青年科技人才托举工程、中华中医药学会青年人才托举工程A类项目(No. 2021-QNRC2-A01)、南京中医药大学自然科学基金青年项目(NZY81903557)、南京中医药大学中药学一流学科开放课题(2020YLXK019)等项目的资助支持。



